Seis temas comuns na prática diária. Todos merecem discussão e ação imediata. A conduta tem de ser acertada para evitar um final trágico.
Adap. do autor Prof. Paulo Barroso Tavares – Coordenador da Disciplina de Cirurgia Pediátrica / HUPE
- A melhor forma de tratar uma apendicite aguda.
- Como diagnosticar e tratar o pneumotórax.
- A melhor abordagem do empiema pleural.
- Como conduzir um trauma abdominal fechado.
- Como diagnosticar e conduzir uma invaginação intestinal.
- Diagnóstico rápido, preciso, com tratamento imediato da torção testicular.
APENDICITE AGUDA
É a causa mais frequente de abdome agudo inflamatório em crianças.
A faixa etária mais comum é entre 4 e 14 anos.
O principal agente desencadeante da apendicite aguda é a obstrução da sua luz.
A causa pode ser um fecalito ou parasitas, sendo comum obstrução da luz por hiperplasia linfoide, nos casos de viroses.
Classificação
- Apendicite simples: edema apendicular, úlceras em mucosa e secreção purulenta na luz.
- Apendicite supurativa: serosa com fibrina, congestão vascular, petéquias com líquido peritoneal claro ou turvo.
- Apendicite gangrenosa: necrose apendicular, microperfuração, evoluindo para ruptura e peritonite franca ou abscesso apendicular.
Diagnóstico
História e exame físico são fundamentais. Não se pode pensar em diagnóstico de apendicite aguda sem palpar o abdome.
O quadro clínico clássico é de dor abdominal, de início no epigástrio, ou periumbilical, que depois passa para a fossa ilíaca direita, associada a náuseas, vômitos e febre. Fácies de dor. Diarreia ocorre geralmente quando o paciente já está com peritonite.
Recomenda-se solicitar que a criança coloque o dedo indicador no local onde sente a dor, no ponto de McBurney, localizado na fossa ilíaca direita, o que invariavelmente oferece o diagnóstico inicial de apendicite aguda.
A descompressão rápida e dolorosa e a percussão, na fossa ilíaca direita, confirmam o diagnóstico clínico. Sinal de Rovsing, comprimindo o flanco esquerdo com dor reflexa, por distensão de gases na fossa ilíaca direita.
Dificuldade de deambular, perna direita fletida, com queixa de dor ao esticá-la, em posição antálgica, criança quieta, não querendo ser incomodada, sugere mais ainda o diagnóstico.
Há situações, como nos casos de apendicite retrocecal, ou de crianças menores do que 2 a 3 anos, em que o diagnóstico se torna mais complicado. É preciso lançar mão de exames radiológicos para diagnóstico:
- Radiografia simples de abdome, em pé e deitado: apagamento do músculo psoas, presença de alça sentinela, edema de alças, distensão de alças intestinais e fecalito em fossa ilíaca direita.
- Ultrassonografia: diâmetro do apêndice maior do que 6 mm, presença de pus ou líquido periapendicular, abscesso na fossa ilíaca direita, presença de apendicolito.
- Tomografia computadorizada: espessamento do apêndice, maior do que 6 mm, presença de líquido livre em goteira parietocólica ou pelve, infiltração da gordura adjacente, linfonodos e apendicolito.
Exames laboratoriais como hemograma, creatinina, PCR, exames de urina, como cultura e exame simples, ajudam como diagnósticos diferenciais, não como diagnósticos de apendicite aguda.
Diagnósticos diferenciais
São diagnósticos diferenciais: gastrenterite, adenite mesentérica, diverticulite de Meckel, púrpura, epilepsia abdominal, cisto de ovário torcido, colecistite, inflamação pélvica, crise de falcização, constipação intestinal, teflite leucêmica, contratura muscular.
Tratamento
- Suspensão da dieta oral.
- Hidratação venosa, com reposição de líquidos (nos casos de vômito ou diarreia).
- Analgesia.
- Antibiótico endovenoso.
Os esquemas antibióticos: dependem da fase da apendicite aguda. É fundamental iniciar o tratamento com antibiótico antes do início da cirurgia, com objetivo de reduzir a incidência de infecção de ferida operatória e de abscesso intra-abdominal.
Esquema da antibioticoterapia
- Fase edematosa: amoxicilina e clavulanato de potássio ou cefoxitina.
- Fase fibrinopurulenta ou gangrenosa: ampicilina, gentamicina e metronidazol; piperacilina e tazobactan; ceftriaxone e metronidazol; ou ciprofloxacino e metronidazol.
Apendicectomia
Laparotomia x laparoscopia.São vantagens da laparoscopia:
- A localização mais rápida e fácil do apêndice.
- Aspiração e lavagem dos recessos cavitários, sem necessidade de grande incisão, fato comum em crianças grandes ou obesas, quando submetidas à laparotomia.
- Permite inspeção geral da cavidade.
- Fornece diagnóstico preciso.
- Menor contaminação da ferida operatória.
Desvantagens da laparoscopia:
- Custo mais elevado (controverso).
- Investimento financeiro na aparelhagem.
Nas fases precoces, principalmente em crianças magras, a incisão pequena e única na fossa ilíaca direita é a mais aceita pela grande maioria dos cirurgiões pediátricos e pelas famílias.
PNEUMOTÓRAX
Situações que ocasionem um processo de aumento brusco da pressão alveolar ou prolongamento do tempo de gradiente pressórico máximo podem causar ruptura de alvéolos.
A obstrução parcial de bronquíolos ou de pequenos brônquios pode criar mecanismo valvular, com distensão de alvéolos e também causar pneumotórax quando houver concomitante ruptura da pleura visceral.
Ar no espaço subpleural causa enfisema subpleural. Ar causando dissecção das bainhas dos vasos sanguíneos provoca pneumomediastino ou enfisema intersticial. Em direção do pericárdio ocasiona pneumopericárdio. Nos tecidos moles, causa enfisema subcutâneo.
O pneumotórax sintomático tem de ser drenado. Causas comuns de pneumotórax são manobras de ressuscitação, aspiração de mecônio, atelectasias, membrana hialina, pneumonia necrotizante, complicações de punção venosa (veia jugular e subclávia), ruptura de pneumatocele, corpo estranho, asma e pneumotórax espontâneo.
Ocorre mais comumente em crianças submetidas à intubação endotraqueal, com pressão positiva alveolar contínua (CPAP), associada à pressão expiratória positiva final (PEEP). Acontece também em casos de perfuração de brônquio por cateter de aspiração.
O diagnóstico se dá em crianças apresentando palidez, cianose, abaulamento e timpanismo torácico, desvio do ictus, murmúrio vesicular muito diminuído ou ausente, queda dos níveis de saturação e até parada cardíaca.
A confirmação se dá pela radiografia simples de tórax, com aparecimento da linha da pleura visceral, em maior ou menor intensidade de pneumotórax. Pode ou não causar desvio do mediastino e rechaço do diafragma ipsilateral.
EMPIEMA PLEURAL
É o acúmulo de secreção purulenta no espaço pleural. Pode ser septado por fibrina ou ocupar todo o espaço pleural. Desenvolve-se por pneumonia bacteriana, após trauma, perfuração de esôfago, após toracotomia ou, mais raramente, por infecção bacteriana primária.
O empiema ocorre por diversos fatores. Infecção do parênquima pulmonar, baixa resistência natural, agressividade do micro-organismo. Há acúmulo de líquido no espaço pleural por aumento da pressão coloidosmótica dos transudatos inflamatórios e alteração da permeabilidade capilar dos processos inflamatórios. Os micro-organismos atingem o espaço pleural, transformando o derrame pleural de seroso para fibrinoso, ou seja, empiema pleural.
Nas crianças com pneumonia, ocorre empiema pleural em 0,6 a 2% dos casos. Naquelas que necessitam de internação, pode ocorrer em cerca de 40% dos casos. Em 70% dos casos, não se identifica a bactéria causadora da pneumonia.
Os agentes mais comuns são Staphylococcus aureus, Streptococcus pneumoniae e Haemophilus influenzae. Nos casos de tuberculose pulmonar o líquido pleural em geral é seroso, citrino.
Na fase inicial, o derrame pleural é seroso, citrino, passando para a fase fibrinopurulenta, com fibrina, ocupando todo o espaço pleural. Em geral, após o tratamento, evolui sem sequelas. Mais raramente evolui para encarceramento pulmonar, formando paquipleuris, exigindo decorticação pulmonar.
Quando ocorre pneumonite necrosante com pneumotórax e empiema pleural, há necessidade de drenagem cirúrgica.
O diagnóstico é inicialmente clínico, com ausência do frêmito toracovocal, murmúrio vesicular ausente e macicez à percussão. A seguir a radiografia de tórax revela desaparecimento do seio costofrênico e velamento da base pulmonar ou de todo o hemitórax.
A ultrassonografia torácica e a tomografia computadorizada do tórax são importantes para auxílio nos casos de diagnóstico mais complexo. Por meio desses exames localizam-se lojas, septações, e afere-se o volume, ajudando, portanto, na decisão do tratamento.
A toracocentese dá a certeza do diagnóstico e pode ser o tratamento cirúrgico definitivo, nos casos de secreção serosa, fluida, transparente e de pequeno volume. Envia-se o material para cultura e antibiograma. É realizada no 5º ou 6º espaços intercostais, rente ao bordo superior da costela.
Nos casos de secreção purulenta, recomenda-se a toracostomia (drenagem pleural). A videotoracoscopia, por sua vez, tende a ser usada nos pacientes com empiema pleural.
Realiza-se a limpeza do conteúdo purulento, coloca-se o dreno sobre visão direta, resultando na redução do tempo de internação. As desvantagens seriam haver duas incisões na pele, maior custo (o que é discutível), e a alta frequência de bons resultados nas drenagens convencionais.
Na ausência de saída de secreção, ou clareamento, sem obstrução, retira-se o dreno pleural. O tempo de drenagem é variável de caso a caso.
Nos casos de empiemas complicados, com septações, áreas necróticas ou lojas empiemáticas não drenadas, há necessidade de nova intervenção cirúrgica. O melhor acesso é por videotoracoscopia.
A drenagem aberta é realizada nos casos de fístula bronca pleural, com total expansão pulmonar, após 10 dias de drenagem fechada com pulmão aderido ao gradil costal.

TRAUMA ABDOMINAL FECHADO
Os traumas abdominais mais comuns em crianças são os decorrentes de atropelamentos, acidentes automobilísticos e ciclísticos. O trauma abdominal isolado é raro, em geral há outras lesões, como os traumatismos cranianos.
O impacto direto acomete mais as vísceras maciças. Baço e fígado são os locais mais comumente atingidos. Após abordagem inicial do trauma, com monitorização adequada, avaliamos contusões abdominais, fratura de costelas ou de ossos da pelve, as quais causam dor abdominal, sem a ocorrência de abdome agudo. Irritação peritoneal e hematúria são sinais indicativos de lesão de órgãos abdominais.
A laparotomia deve ser realizada em crianças com expansão do volume abdominal, sem estabilização hemodinâmica, necessitando de reposição sanguínea superior a 40 ml/kg, com sinais claros de peritonite.
Nas crianças com estabilidade hemodinâmica e suspeita de lesão de órgãos abdominais, realizam-se exames de imagem. A maior parte das crianças se beneficia com o tratamento conservador do hemoperitôneo. A tomografia computadorizada do abdome com contraste venoso é o melhor método diagnóstico.
A unidade hospitalar necessita de monitorização adequada, hematócrito seriado, equipe cirúrgica 24 h, banco de sangue e radiologia 24 h.
Após o trauma abdominal fechado, quando houver instabilidade clínica, estará indicada de imediato a laparotomia. No caso de estabilidade hemodinâmica, realiza-se a tomografia computadorizada, com contraste. Se houver lesões como pneumoperitônio, perfuração de vias urinárias e transecção do pâncreas, a laparotomia também estará indicada de imediato. Nos casos de lesões de baço e fígado, deve-se atentar principalmente às condições clínicas, a despeito das lesões diagnosticadas na tomografia. Dessa forma, evita-se a laparotomia indicada apenas pelo achado radiológico. O mais importante, portanto, é a avaliação clínica.
Quando o tratamento clínico não alcança o resultado esperado, e há deterioração clínica, indica-se a laparotomia.
INVAGINAÇÃO INTESTINAL
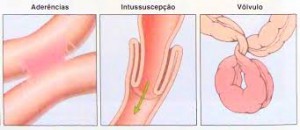
Doença característica do lactente saudável, que começa a apresentar irritabilidade e dor do tipo cólica.
Ocorre mais comumente do 3º ao 9º mês de vida. A forma mais comum é a invaginação íleo-ceco-cólica.
O segmento de alça intestinal penetra no segmento distal, causando isquemia, distensão abdominal e massa palpável.
A invaginação primária ocorre em 90% dos casos.
A causa é desconhecida.
Os casos de invaginação secundária são mais comuns após os 2 anos de idade.
A “cabeça de invaginação” é secundária a uma doença. São comuns o divertículo de Meckel, os cistos enterógenos, o linfoma, os pólipos e os tumores do intestino delgado.
O quadro clínico caracteriza-se por dor abdominal do tipo cólica, palidez cutânea, vômitos e irritabilidade.
Após o fim dos sintomas, ocorre novamente dor abdominal. Em seguida, há eliminação de muco com sangue (aspecto de geleia de morango) e massa tumoral (aspecto de chouriço).
No toque retal, evidencia-se sangue nas fezes ou muco com sangue. Se não houver tratamento nessa fase da doença, ocorrem obstrução intestinal e choque séptico.
A radiografia de abdome ajuda nos casos de obstrução intestinal. Para diagnóstico, contudo, a ultrassonografia de abdome é o exame de escolha. Observa-se imagem em “alvo” ou “pseudorrim”. A imagem é fruto do intestino invaginado por dentro do outro.
O enema oferece o diagnóstico e pode tratar a criança sem cirurgia. Até 24 h de doença, há possibilidade de redução da invaginação pelo clister. O mesmo processo pode ser realizado por meio de clister opaco, com intensificador de imagem, ou por soro morno, acompanhado de ultrassonografia abdominal.
Há contraindicações na realização de redução hidrostática. Não realizar em casos de sinais de perfuração, peritonite e obstrução intestinal, assim como em crianças com casos graves, com tempo de evolução maior do que 48 h, nas invaginações crônicas e naquelas com mais de dois anos de idade.
O tratamento cirúrgico se impõe quando há falha no tratamento clínico. Também é recomendado nos casos de invaginação crônica, em pós-operatório de cirurgia abdominal, em crianças com mais de 2 anos e recém-nascidos.
TORÇÃO TESTICULAR
Torção testicular é uma verdadeira emergência cirúrgica. Toda criança com dor testicular de início súbito e com edema em bolsa escrotal tem de ser examinada imediatamente.
A idade da criança é fator a ser considerado. A torção pode ocorrer em qualquer época, mais é comum nos recém-nascidos e nos estágios iniciais da puberdade. A torção dos apêndices testiculares é mais comum nos pré-púberes, enquanto a epididimite ocorre mais em adolescentes.
Dor intensa e de início súbito é mais comum na torção testicular. Dor leve ou moderada, com aumento gradual, ocorre mais nas torções de apêndices testiculares e na epididimite.
Na torção testicular, são comuns náusea e vômitos. Já na epididimite, são mais frequentemente observados febre e sintomas urinários, assim como história de bexiga neurogênica, anomalias geniturinárias congênitas e exploração uretral.
Exame físico na torção testicular revela eritema e edema de bolsa escrotal unilateral, testículo elevado ou em situação transversal, aumento do volume testicular, dor intensa à palpação, reflexo cremastérico ausente no lado afetado e espessamento da pele escrotal, com edema importante.
Na torção testicular, todo o testículo fica dolorido. Na torção do apêndice testicular, pode ser observada uma coloração azulada no ápice testicular, também conhecido como sinal do ponto azul. Nesse ponto, pode ser examinado um nódulo doloroso, que é o apêndice torcido.
Diagnósticos diferenciais são: a púrpura de Henoch-Schönlein, traumatismo do escroto, hérnia inguinal, hidrocele e varicocele.
Nem sempre é fácil chegar ao diagnóstico pela história e pelo exame físico. Recorre-se aos exames de imagem, sendo estes os mais comuns: cintilografia e ultrassonografia com Doppler.
A cintilografia com tecnécio é precisa quanto à má perfusão testicular em até 90% dos casos. Não é um exame de fácil realização, porque em geral não está disponível nos serviços de emergência. Como o diagnóstico precisa ser concluído com máxima brevidade, ele não deve ser usado como rotina.
Ultrassonografia com Doppler é o exame de escolha para diagnóstico da torção testicular. Esse exame informa o fluxo sanguíneo do testículo normal, assim como o fluxo sanguíneo da parede escrotal e o intratesticular do testículo torcido. Caso esteja normal ou aumentado, exclui-se a possibilidade torção. Caso esteja com fluxo diminuído ou ausente, há torção testicular.
Nos casos em que não houver possibilidade de realização de exames, ou quando houver dúvida diagnóstica, sempre estará indicada a exploração cirúrgica. A cirurgia deverá ser realizada de imediato nos casos de torção testicular.
REFERÊNCIAS BIBLIOGRÁFICAS
- Johnson EM. Complications and risks of central venous catheter placement in children. Surgery.1988 Nov, 124(5):911-6.
- Cruzeiro PC. Central venous catheter placement in children: a prospective study of complications in a Brazilian public hospital. Pediatr Surg Int. 2006 Jun; 22(6):536-40.
- Rey C. Mechanical complications during central venous cannulations in pediatric patients. Intensive Care Med. 2009 Aug, 35(8):1438-43.
- O’ Lone E. Spontaneous pneumothorax in children: when is invasive treatment indicated? Pediatr Pulmonol. 2008;43(1):41-6.
- Bialas RC. Video-assisted thoracic surgery for primary spontaneous pneumothorax in children: is there an optimal technique? J Pediatr Surg. 2008;43(12):2151-5.
- Pillai D. Implementation and impact of a consensus diagnostic and management algorithm for complicated pneumonia in children. J Investig Med. 2011 Dec; 59(8):1221-7.
- Ghritlaharey RK.Tube thoracostomy: Primary management option for empyema thoracic in children. Afr J Pediatr Surg.2012 Jan; 9(1):22-6.
- Cobanoglu U. Comparison of the methods of fibrinolysis by thoracostomy and thoracoscopic decortications in children with stage II and III empyema: a prospective randomized study. Pediatr Rep. 2011 Sep 30;3(4):e29.
- Podkamenev VV. Treatment of closed spleen injuries with intraabdominal bleeding in children. Khirurgiia (Mosk). 2010;(4):47-50.
- Diéguez EV. Biloma as a complication after closed abdominal trauma. Review of the literature after bile leaks. Cir Pediatr. 2009 Jul; 22(3):1668-71.
- Lane WG. Screening for occult abdominal trauma in children with suspected physical abuse. Pediatrics. 2009 Dec; 124(6):1595-602.
- Trout AT. A critical evaluation of US for the diagnosis of pediatric acute appendicitis in a real-life setting: how can we improve the diagnostic value of sonography? Pediatr Radiol. 2012 Mar 9.
- Nataraja RM. Comparison of intraabdominal abscess formation after laparoscopic and open appendicectomies in children. J. Pediatr Surg. 2012 Feb; 47(2):317-21.
- Myers AL. Hospital cost analysis of a prospective, randomized trial of early vs. interval appendectomy of perforated appendicitis in children. J Am Coll Surg. 2012 Feb 16.
- St. Peter SD. Single daily dosing ceftriaxone and metronidazole vs. standard triple antibiotic regimen for perforated appendicitis in children: a prospective randomized trial. J Pediatr Surg. 2008 Jun; 43(6):981-5.
- Applegate KE. Clinically suspected Intussusception in children: evidence-based review and self-assessment module. AJR Am J Roentgenol. 2005 Sep; 185(3 Suppl):S175-83.
- Ko HS. Current radiological management of Intussusception in children. Eur Radiol, 2007 Sep; 17(9):2411-21.
- Navarro O. The impact of imaging in the management of Intussusception owing to pathologic lead points in children. A review of 43 cases. Pediatr Radiol. 2000 Sep; 30(9):594-603.
- Daneman A. Intussusception on small bowel examinations in children. AJR Am J Roentgenol. 1982 Aug; 139(2):299-304.
- Ein SH. Hydrostatic reduction of intussusceptions caused by lead points. J Pediatr Surg. 1986 Oct; 21(10):883-6.
- Boettcher M. Clinical predictors of testicular torsion in children. Urology. 2012 Mar; 79(3):670-4.
- Ciftci AO. Clinical predictors for differential diagnosis of acute scrotum. Eur J Pediatr Surg. 2004 Oct; 14(5):333-8.
- Campobasso P. Acute scrotum in children: analysis of 265 consective cases. Pediatr Med Chir. 1994 Nov-Dec; 16(6):521.
- Stehr M. Critical validation of color Doppler ultrasound in diagnostic of acute scrotum in children. Eur J Pediatr Surg. 2003 Dec; 13(6):386-92.
http://revistadepediatriasoperj.org.br/detalhe_artigo.asp?id=617
http://www.cipe.org.br/

achei o documento interessante e quero forneça me conteudo deste ,sou enfermeiro , e acho esta documento uma mais valia.
Olá, como vai ?
Interessante sua puplicação vc acha pertinente colocar
neste meu site?
lhttp://planosdesaudehdm.com.br
.
Um grande abraço.
Aqui é a Nicole De Oliveira , gostei muito do seu artigo tem
muito conteúdo de valor, parabéns nota 10.